O Fantástico Mundo da Epigenética
Organismos pluricelulares, como o nosso, são formados por muitos tipos de células, sendo que praticamente todas elas possuem a mesma quantidade e os mesmos tipos de DNA. Entretanto, aí vem a pergunta:
“Se temos o mesmo DNA em todas as células, por que elas são diferentes?”
Na verdade, o que ocorre, é que genes expressos (ativos) em alguns tecidos podem estar inativos (não expressos) em outros. Atualmente sabemos que os genes raramente existem na forma de “DNA puro”, mas sim revestidos e ligados a moléculas que os tornam mais ou menos ativos sem afetar o DNA. Esses revestimentos químicos dos genes podem ser transmitidos durante as divisões celulares, ou seja, são herdáveis.
A epigenética é um termo usado na biologia para se referir as modificações das funções genéticas que são herdadas, mas que por sua vez não alteram a sequência do DNA do indivíduo, ou seja, representa as variações não-genéticas que são trasmitidas de uma geração para outra.
A metilação do DNA
O primeiro mecanismo epigenético foi proposto em 1975, trata-se da metilação do DNA. Esse processo consiste na adição de um radical metil (CH3) no carbono 5 da base nitrogenada citosina que é seguida por uma base guanina. Essa adição é feita por enzimas DNA - metiltransferase (DNMTs). Essas enzimas realizam novas metilações e cuidam da manutação das já realizadas. É importante salientar que a desmetilação pode ocorrer naturalmente ao longo de várias etapas de replicação.
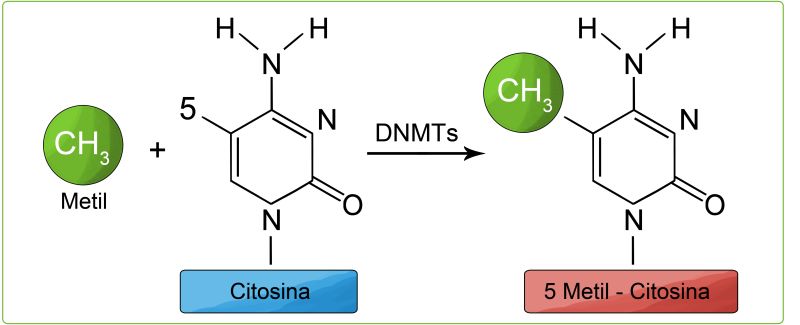
A metilação do DNA leva ao recrutamento de proteínas que causam a compactação da cromatina impedindo que a enzima RNA-Polimerase se ligue a molécula, dessa forma não ocorre a expressão gênica, uma vez que a RNA-Polimerase é a enzima responsável pela transcrição, ou seja, pela síntese de RNA a partir da informação contida na fita de DNA.
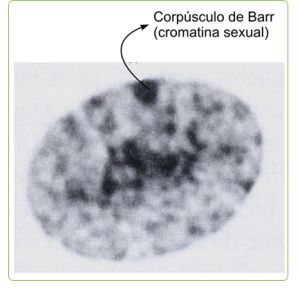
Foto de uma célula feminina vista ao microscópio óptico
A inativação de 85% dos genes de um cromossomo X nas mulheres (processo denominado de “compensação de dose”, uma vez que as mulheres possuem dois cromossomos X), ocorre através da metilação e da compactação do DNA, formando o corpúsculo de Barr (cromatina sexual). Uma região do núcleo das células das mulheres com coloração mais densa, que pode ser observada em microscópio óptico, é nada mais que o cromossomo X inativado. Além da metilação do DNA (marcador epigenético mais estudado) existem outros mecanísmos epigentéticos conhecidos:
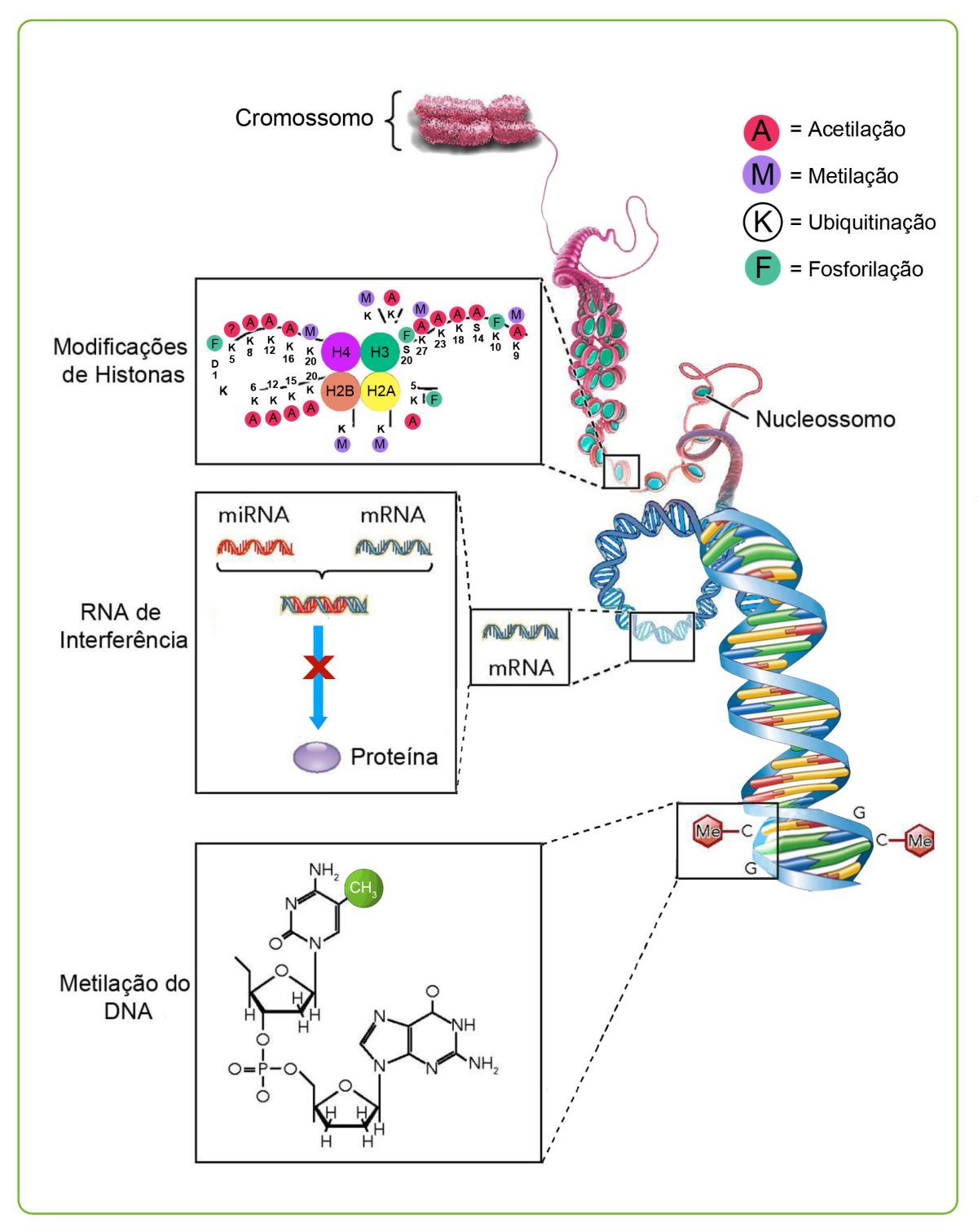
► Modificações covalentes em histonas:
● Acetilação: Adição de um grupo acetil (COCH3). Esse processo abre a cromatina e ativa a transcrição, enquanto que a desacetização condensa a cromatina e impede a transcrição.
● Metilação: Adição de um grupo metil, geralmente esse processo inativa a transcrição, enquanto que a desmetilação ativa.
● Ubiquitinação: Adição de uma proteína denominada ubiquitina que sinaliza que uma determinada proteína alvo, no caso a histona, deve ser degradada.
● Fosforilação: Adição de um grupo fosfato (PO4). O aumento de grupos fosfato nas histonas aumenta a condensação da cromatina, inativando cada vez mais os genes.
► RNAs não codificantes:
Pequenos ou micro RNAs (miRNAs) espalhados ao longo do genoma com função regulatória de controle da expressão gênica. Geralmente ligam-se a mRNA específicos impedindo a produção de uma determinada proteína.
Do genoma ao epigenoma
Se o genoma é o conjunto de genes de um organismo, o epigenoma é o conjunto de modificações químicas que ocorrem no próprio genoma e cromatina. Esse código epigenético é quem dá instruções ao genoma de quando e onde os genes devem ser expressos.
A adição de fatores ambientais nos padrões epigenéticos
Os padrões epigenéticos podem ser afetados por fatores ambientais, tais como alimentação, uso de drogas, exercício físico, stress, etc. Durante a gravidez, por exemplo, esses fatores podem influenciar os mecanismos epigenéticos do embrião/feto. Gêmeos monozigóticos, apesar de terem sido formados a partir de um mesmo zigoto e de possuirem o mesmo material genético, acumulam diferenças conforme envelhecem, uma vez que o ambiente influencia no fenótipo, de tal forma que os padrões epigenéticos de dois irmãos monozigotos não serão idênticos.



Diversos genes em nosso genoma estão associados com a supressão de tumores, participando da regulação da divisão celular e de outros processos vitais para a célula. A mutação de um gene supressor tumoral pode propiciar o surgimento de câncer, da mesma forma, a metilação de um desses genes teria o mesmo efeito.
Padrões epigenéticos de células germinativas
Estudos mostram que alterações nos padrões epigenéticos de células germinativas aparecem nos gametas e podem ser transmitidas para as gerações futuras. Essas alterações estão associadas tanto à exposições ambientais (álcool, tabagismo, nutrição, radiação ionizante, etc), bem como a manipulação de células germinativas ou de embriões concebidos por técnicas de reprodução assistida (fertilização in vitro).

Representação ilustrativa da vulnerabilidade epigenética do espermatozóides ao estilo de vida e fatores ambientais e seus efeitos transgeracionais no desenvolvimento embrionário, doenças congênitas ao nascimento, e em doenças de início tardio como obesidade, hipertensão, diabetes, entre outras.
Veja a seguir um experimento epigenético:

A Epigenética e a evolução segundo a ideia Neodarwinista, mutações e recombinações gênicas são os principais fatores evolutivos que promovem o aumento da variabilidade genética possibilitando o surgimento de novos genótipos e fenótipos, sendo esses selecionados pelo ambiente.
Os estudos da epigenética mostram que o ambiente também pode ter influência na expressão dos genes durante a vida do indivíduo, promovendo alterações no chamado epigenótipo - Essas alterações herdadas ao longo da vida podem então, ser tranmitidas aos indivíduos das próximas gerações.

https://www.youtube.com/watch?v=owf6TgR_0BY
https://www.youtube.com/watch?v=Amlqnpz2xa8
https://www.youtube.com/watch?v=OYvi46Rm2hU


